III. Ионные механизмы возбуждения
Известно, что возбуждение связано с развитием в нейроне деполяризации. Деполяризационный ответ нейрона на возбуждающую стимуляцию получил название возбуждающего постсинаптического потенциала (ВПСП). Внутриклеточно ВПСП в нейронах млекопитающих был впервые записан Броком, Кумбсом и Экклсом (Brock, Combs a, Eccles, 1952), а еще раньше в мышечном волокне - Фэттом и Катцем (Fatt a. Katz, 1950). Микроэлектродная техника, обеспечившая возможность таких записей, стала за последние 15 лет достоянием многих нейрофизиологических лабораторий мира, и к настоящему времени имеется огромное число работ, посвященных изучению постсинаптических потенциалов (ПСП).
Какие изменения проницаемости должны произойти в мембране нейрона, чтобы при этом возникла деполяризация? Очевидно, должны создаваться условия для увеличения числа катионов или уменьшения числа анионов внутри клетки, что приведет к снижению ее отрицательного заряда. Поскольку изменения проницаемости возникают именно в субсинаптических участках мембраны, направление возникающего в этих частях мембраны тока должно быть входящим (при этом суммарное количество положительных нарядов внутри клетки будет возрастать). В остальных отделах мембраны (внесинаптических или, как принято говорить, постсинаптических) ток будет иметь выходящее направление (рис. 23, II). При прохождении этого тока через постсинаптическую мембрану, обладающую довольно высоким сопротивлением (около 1 Мом), внутри клетки возникает положительный потенциал, который и регистрируется в виде ВПСП (рис. 23, I).
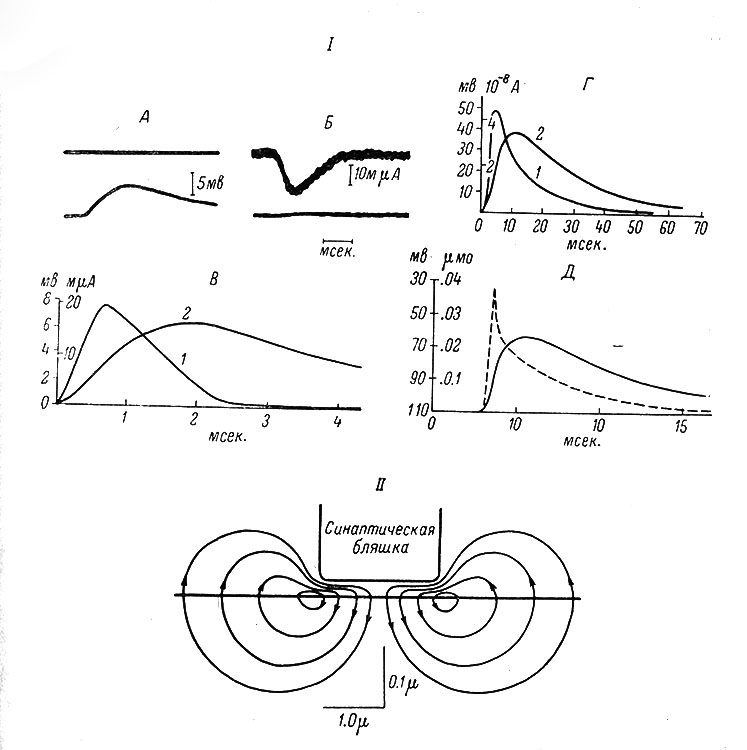
Рис. 23. Развитие во времени ВПСП и генерирующего его тока. (Eccles, 1964). 1. А-В - моносинаптический ВПСП, отведенный внутриклеточно от мотонейрона спинного мозга кошек. А: нижняя кривая - запись ВПСП, верхняя кривая - запись второго луча осциллографа, включенного для записи постсинаптического трансмембранного тока. Б: верхняя кривая - запись тока, необходимого для фиксации мембранного потенциала на уровне потенциала покоя при развитии ВПСП; нижняя кривая - зафиксированный мембранный потенциал. В - ВПСП (2), представленный на А, и возбуждающий постсинаптический ток (1), представленный на Б, но противоположного по отношению к фиксирующему току направления (Araki a. Terzuolo, 1962). Г - ВПСП (2) и генерирующий его постсинаптический ток (1), возникающий при моносинаптической активации клетки сердечного ганглия омара (Hagivara, Watanabe a. Saito, 1959). Д - ВПСП и шунтирующая проводимость активированной субсинаптической мембраны (прерывистая линия) при моносинаптической активации цилиарного ганглия цыпленка (Martin a. Pilar, 1963). 11 - схематическое изображение активированной возбуждающей синаптической бляшки, субсинаптической и постсинаптической мембраны (Экклс, 1957)
Существует несколько экспериментальных подходов для выяснения ионных механизмов нейронного возбуждения (ВПСП).
В период увеличения проницаемости субсинаптических зон часть ионов вне- и внутриклеточной среды начинает диффузионно перемещаться по своим электрохимическим градиентам, в результате чего уровень МП будет изменяться до тех пор пока не возникнет новое динамическое равновесие распределения ионов, при котором потенциал клетки не будет претерпевать дальнейших изменений. Этот "новый" потенциал, при котором ионный механизм, срабатывающий при активации возбуждающей субсинаптической мембраны, не вызывает изменения поляризации клетки (развития ВПСП), получил название потенциала равновесия ВПСП (EВПСП). EВПСП по существу является тем напряжением, которое обусловливает возникновение ионных токов, лежащих в основе развития ВПСП при нормальной поляризации клетки. Такое представление является, конечно, абстракцией, поскольку непосредственными силами, побуждающими перемещение ионов, являются существующие в "покое" электрохимические градиенты. До синаптической активации относительно низкая проницаемость "покоящейся" мембраны ограничивает кинетические возможности электрических и концентрационных потенциалов. Активированная мембрана резко уменьшает свое сопротивление прохождению ионов, и электрохимические градиенты реализуют свою энергию в кинетическом перемещении ионов через мембрану. Идеальным концом этого процесса было бы новое состояние электрохимического равновесия при уровне МП, равном EВПСП. Однако ввиду кратковременности возбуждающей активации субсинаптических мембран, а также вследствие того, что при определенном уровне деполяризации в нейроне развивается импульсная активность,* синаптическая деполяризация никогда не достигает EВПСП. В экспериментальных условиях эту величину можно определять с достаточной точностью.
* (Закономерности развития и ионные механизмы импульсной активности описываются ниже.)
Для этого обычно используется искусственное изменение уровня МП с помощью пропускания тока от внешнего источника через один из каналов двухканального микроэлектрода. Второй его канал, как обычно, используется для регистрации потенциалов. Такие опыты были поставлены на мотонейронах (МН) млекопитающих (Coombs, Eccles a. Fatt, 1955c) и земноводных (Araki, 1960), нейронах сердечного ганглия омара (Hagiwara, Watanabe a. Saito, 1959), симпатического ганглия лягушки (Nishi a. Koketsu, 1960) и некоторых других клетках. Полученные данные оказались сходными в том отношении, что во всех указанных нейронах величина ВПСП изменялась прямо пропорционально уровню МП. Однако нулевая величина ВПСП в различных клетках имела место при различных уровнях МП, т. е. EВПСП в нейронах разного типа был неодинаковым. Например, в клетках симпатического ганглия лягушки ВПСП становился равным 0 при величине МП порядка -14 мв, а в МН кошки при нулевом МП (рис. 24). Дальнейшее уменьшение МП (что может сопровождаться изменением его знака) ведет к реверсии знака ВПСП, т. е. к превращению его в гиперполяризационный потенциал.
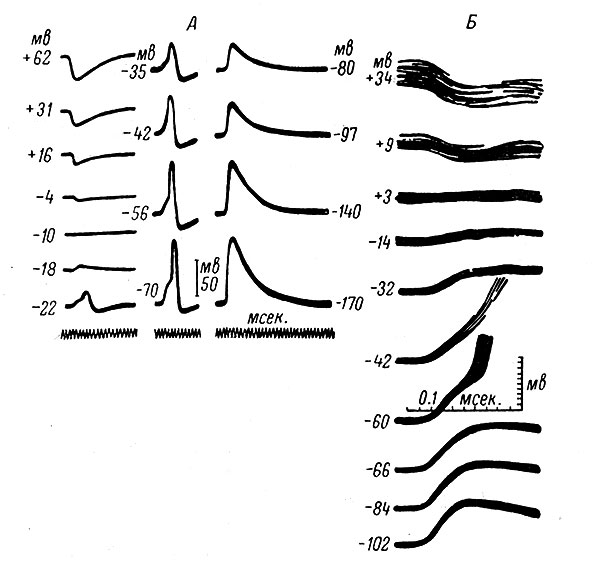
Рис. 24. Зависимость величины ВПСП от уровня мембранного потенциала. (Eccles, 1964). А - серия ВПСП, вызванных в клетке симпатического ганглия лягушки. Мембранный потенциал изменяется с помощью пропускания постоянного электрического тока через записывающий электрод с уровня покоя (-70 мв) до уровней, обозначенных в мв рядом с каждой записью. Наблюдается потенциал действия при уровнях от -22 до -70 мв. Температура 24-26°С (Nishi a. Koketsu, 1960). Б - ВПСП, вызванные в мотонейроне ядра n. biceps-semitendinosus при различных уровнях мембранного потенциала, указанных слева от записей. Каждая запись - 20 одиночных пробегов луча. Мембранный потенциал изменялся до указанных значений с помощью постоянного тока, пропускаемого через второй канал двухканального микроэлектрода. Исходный уровень составлял -66 мв (Coombs, Eccles a. Fatt, 1955c)
На нервно-мышечном соединении с помощью методики фиксации МП было также показано, что токи концевой пластинки (ТКП), как и потенциалы концевой пластинки (ПКП), изменяются пропорционально величине МП мышечного волокна (Takeuchi а. Таkeuchi, 1959, 1960). Прямая зависимость между величиной МП постсинаптической клетки и величиной ВПСП, ПКП и ТКП, а также их реверсия при определенном уровне МП, указывают на то, что во время возбуждающей синаптической активации все ионы движутся по своим электрохимическим градиентам, т. е. в соответствии с физико-химическими закономерностями.
Какие ионы могут принимать участие в генерации ВПСП? Для выяснения этого вопроса можно использовать два экспериментальных приема. Первый заключается в том, что если менять внешнюю концентрацию того или иного иона, изменяя тем самым потенциал равновесия, и следить при этом за изменениями EВПСП то можно определить степень участия данного иона в создании деполяризационного процесса. Кроме того, используется замена одних ионов другими, обладающими иными величинами диаметров гидратных оболочек, что позволяет составить суждение о степени изменения проницаемости субсинаптической мембраны при развитии ВПСП. Второй прием заключается в том, что с помощью электрофоретической инъекции определенного иона через один из каналов двухканального микроэлектрода можно изменять его внутреннюю концентрацию, а следовательно, и потенциал равновесия, и далее на этом фоне изучать характер изменения величины ВПСП и EВПСП. Оба метода имеют ряд ограничений. Осуществление первого возможно только в опытах на изолированных объектах (обычно это нервные клетки холоднокровных или нервно-мышечный препарат), когда имеется возможность изменять концентрацию ионов в окружающей среде. Этот прием не может быть использован для изучения нейронов ц. н. с. млекопитающих. При использовании второго метода пока не существует возможностей для точного определения изменений внутриклеточной концентрации ионов, тем более что при электрофоретической инъекции возникает интенсивный обмен ионов между внутри- и внеклеточной средой. Поэтому пока наиболее точные эксперименты осуществлены на нервно-мышечном соединении скелетной мышцы лягушки.
Было показано, что замена в омывающей среде ионов хлора на ионы глутамата, для которого активированная мембрана практически непроницаема, не меняет потенциала равновесия ТКП. В то же время изменение наружной концентрации ионов калия или натрия существенно влияют на EТКП скелетной мышцы лягушки (Takeuchi a. Takeuchi, 1960). Эти экспериментальные данные позволяют считать, что в основном формирование ТКП осуществляется за счет участия К+ и Na+, причем доминирует в этом процессе увеличение проводимости (проницаемости) для Na+, что и обусловливает деполяризацию. Замена ионов натрия на ионы аммония даже увеличивает величину ПКП (Furukawa, Takagi a. Sugihara, 1956; Nastuk, 1959). Натрий может быть также заменен метил- и этиламмонием (Furukawa a. Furukawa 1959), однако при использовании более крупных катионов (триметилэтиламмоний, холин, диметилэтаноламмоний) деполяризационный процесс значительно снижается (Nastuk, 1959). Таким образом, увеличение проницаемости субсинаптической мембраны имеет известные пределы. По-видимому, диаметр "пор", возникающих при действии медиатора, не превышает двойного диаметра гидратированного иона К+ (Eccles, 1964).
Исследования с электрофоретической инъекцией различных ионов в МН (Coombs, Eccles a. Fatt, 1955c; Araki, Ito a. Oscarsson, 1961, и др.) показали, что ВПСП не меняет при этом существенно своих параметров. Он может несколько уменьшаться по амплитуде, если электрофоретическая инъекция приводит к снижению МП (например, при введении Na+), и во всех случаях его потенциал равновесия приблизительно равен нулю. Все это позволяет считать, что при возбуждающей синаптической активации субсинаптическая мембрана МН делается проницаемой для всех видов ионов, диаметр которых не превышает двойного диаметра К+, главным образом для К+, Na+ и Сl-.
Удельный вес участия этих ионов в деполяризационном процессе остается невыясненным. Возможно, что, как и в случае нервно-мышечного соединения, ионы Сl- не принимают значительного, участия в ионообменных процессах при развитии ВПСП. Однако, если допустить, что все три иона (К+, Na+ и Cl-) участвуют в этих процессах, то все же основная роль в создании деполяризации должна принадлежать Na+. Действительно, при увеличении проницаемости мембраны к К+ этот ион будет выходить из клетки, поскольку его электрохимический градиент направлен наружу (концентрационный градиент для калия доминирует над электрическим). Выход К+ из клетки будет вызывать не де-, а гиперполяризацию. Не может способствовать деполяризационному процессу и движение Сl-. Если принять, что его потенциал равновесия ЕCl равен - 70 мв (Экклс, 1957), то при снижении МП клетки ниже этого уровня ионы Сl- будут поступать внутрь клетки из окружающей среды и создавать гиперполяризацию. Повышение проницаемости к Сl- лишь увеличит этот процесс. Таким образом, только поступление внутрь клетки ионов Na+ создаст деполяризацию. Интенсивность натриевого потока внутрь клетки должна быть высока, чтобы не только противодействовать гинерполяризационным влияниям К+ и Сl-, но и создавать "чистую" деполяризацию.
То, что во время развития ВПСП проводимость мембраны для Na+ значительно больше, чем для К+, действительно показано в опытах на нервно-мышечном соединении (Takeuchi a. Takeuchi, 1960). Что касается МН млекопитающих, то этот вопрос еще ждет своего экспериментального подтверждения. Нельзя, конечно, полностью пренебрегать участием и других низкомолекулярных ионов (Н+, НСО3- и др.) в создании деполяризующих ионных потоков. Однако степень участия этих ионов в механизмах генерации ВПСП совершенно не изучена.*
* (Имеются указания на возможное участие ионов Са++ в генерации ПКП (Nastuk, 1959).)
Таким образом, в основе нейронного возбуждения лежит резкое увеличение проницаемости субсинаптической мембраны по отношению ко всем низкомолекулярным ионам внутри- и внеклеточной среды. Указанное увеличение проницаемости можно расценивать как шунтирование мембраны (Fatt a. Katz, 1951; Castillo a. Katz, 1954c, и многие другие). Действительно, проводимость активированной мембраны в тысячи раз больше проводимости "покоящейся" и в несколько раз больше ее проводимости во время развития потенциала действия (Fatt a. Katz, 1951).
ПОИСК:
© ANFIZ.RU, 2011-2022
При использовании материалов сайта активная ссылка обязательна:
http://anfiz.ru/ 'Анатомия и физиология человека'
При использовании материалов сайта активная ссылка обязательна:
http://anfiz.ru/ 'Анатомия и физиология человека'