Глава 3. Ионные механизмы возбуждения и торможения (Г. А. Вартанян)
I. Мембранный потенциал
Различная концентрация веществ внутри и вне клетки является одним из важнейших признаков жизни. Всякая клетка, находящаяся в полном концентрационном равновесии с окружающей ее средой, мертва. Правда, многие вещества, в первую очередь вода, проникают в клетку по градиенту их концентраций. Однако имеется огромное количество веществ, не следующих этому правилу.
Если разделить различные вещества на классы в соответствии с их проницаемостью, то среди них можно выделить следующие основные группы. Неполярные вещества, характеризующиеся равномерным распределением электронов между атомами, образующими молекулу. Неполные полярные соединения, в которых электроны, связывающие атомы, больше притягиваются к одному из них, вследствие чего молекула превращается в диполь. Ионные соединения, или электролиты, где валентные электроны связаны лишь с одним из атомов или радикалов. В средах, обладающих высокой диэлектрической постоянной, эти связи сильно ослабляются, и отдельные части молекулы ведут себя как самостоятельные ионы. Здесь происходит диссоциация электролита на ионы: положительные - анионы и отрицательные - катионы.
Оставив в стороне вопрос о проникновении в клетку соединений двух первых классов, остановимся более подробно на характере проникновения и распределения различных ионов между клеткой и окружающей ее средой, поскольку именно это распределение лежит в основе мембранного потенциала (МП) клетки.
В настоящее время экспериментально доказано, что содержимое клетки заряжено отрицательно по отношению к ее наружной поверхности и окружающей среде. Этот заряд неодинаков у различных клеток и в большинстве случаев колеблется в пределах от -50 до -100 мв (табл. 9). Наличие электрического заряда указывает на неодинаковое распределение электролитов по обе стороны клеточной поверхностной мембраны, которое принято называть ионной асимметрией.
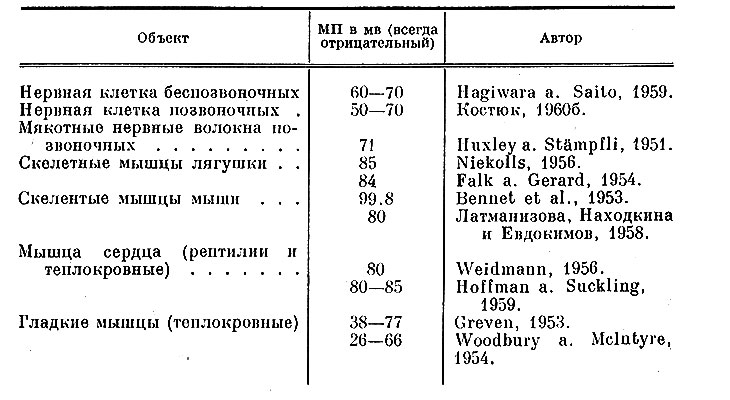
Таблица 9. Величины мембранных потенциалов (МП) различных возбудимых клеток (по Латманизовой, 1965)
Каким образом возникает ионная асимметрия по разные стороны клеточной мембраны? Для выяснения этого вопроса следует хотя бы в общей форме рассмотреть поведение электролитов при прохождении через любую полупроницаемую перепонку.
Все растворенные вещества, в том числе и ионизированные, перемещаются (в случае неравномерного распределения в растворе) согласно градиенту концентрации от участков с более высокой концентрацией к участкам с меньшей концентрацией. Если участки раствора с неодинаковой концентрацией разделены какой-либо мембраной, то диффузия растворенных веществ более или менее замедляется. Ионные компоненты растворенных электролитов - анионы и катионы - нередко обладают разной проницаемостью, а следовательно, и разной подвижностью. Это связано с размерами и конфигурацией ионов, а также с величиной их гидратных оболочек. Например, образующиеся при диссоциации поваренной соли катион Na+ и анион Сl- обладают различной подвижностью. Подвижность и проницаемость Na+ гораздо ниже, чем Сl-. Это соответствует размерам их гидратированных диаметров 2.14 Å для Сl- и 3.4 Å для Na+. При диффузионном проникновении через мембрану из района более высокой концентрации электролита в район меньшей его концентрации ионы Сl- будут переходить на другую сторону мембраны гораздо скорее ионов Na+, так что одна из ее поверхностей на некоторое время зарядится положительно, а другая - отрицательно.
Если мембрана окажется проницаемой только для ионов Сl- и непроницаемой для ионов Na+, то возникает уже не временная, а постоянная разность потенциалов между растворами по обе стороны мембраны. Такая разность потенциалов носит название концентрационной разности потенциалов и может быть рассчитана по уравнению Нернста:
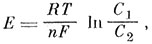
где Е - разность потенциалов, в мв; R - газовая постоянная; Т - абсолютная температура; n - валентность; С1 - более высокая, С2 - более низкая из двух концентраций; F - число Фарадея.
Приведенные закономерности касаются того случая, когда находящиеся по обе стороны полупроницаемой мембраны растворы содержат одни и те же ионы, но в разных концентрациях.
Однако, как известно, протоплазма клетки и внеклеточной жидкости различаются не только по концентрациям, но и по составу ионов, поэтому представления о концентрационном потенциале недостаточны для объяснения событий, разыгрывающихся в районе клеточной мембраны.
Рассмотрим упрощенный случай, более близкий к реальным соотношениям электролитов в клетке. Допустим, что некая мембрана разделяет два разных электролита NaCl и КСl одинаковой концентрации:
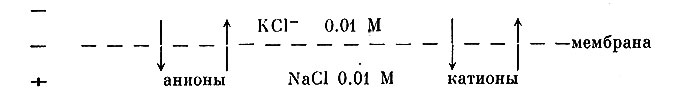
Допустим также, что эта мембрана проницаема как для анионов Сl-, так и для обоих катионов, однако ее проницаемость для К+ значительно выше, чем для Na+. Тогда К+ как более подвижный ион распределяется равномерно по обе стороны мембраны гораздо скорее, чем Na+, и на все время оставания в уравнивании концентраций Na+ одна из сторон мембраны, а именно та, где первоначально находился NaCl, зарядится положительно по отношению к противоположной стороне. Возникающий таким путем потенциал принято называть химическим потенциалом. Если бы мембрана была полностью непроницаемой для Na+, то этот потенциал стал бы постоянным.
В случае клеточного МП все процессы носят гораздо более сложный характер. Прежде всего электролитный состав внутриклеточной и внеклеточной среды довольно сложен и, помимо КCl и NaCl, содержит ряд других ионов, среди которых особенно важную роль в создании мембранного потенциала играют крупные органические анионы, неспособные проникать через клеточную оболочку. Приблизительные концентрации различных ионов в мышечной клетке млекопитающих приведены в табл. 10.
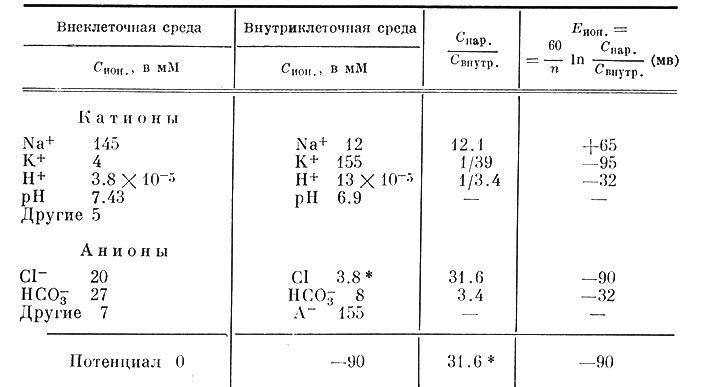
Таблица 10. Приблизительные концентрации ионов и потенциалы равновесия в мышечном волокне млекопитающих и внеклеточной жидкости (по J. W. Woodbury, 1963)
* (Рассчитано по мембранному потенциалу с помощью уравнения Нернста.)
Как видно из таблицы, внеклеточная среда характеризуется относительно высокой концентрацией ионов Na+ и Сl- и низкой концентрацией ионов К+. Внутриклеточная среда, наоборот, содержит незначительные количества Na+ и Сl-, но отличается высоким содержанием К+. Кроме того, внутри клетки содержится свыше 150 мМ высокомолекулярных органических анионов А- на 1 л внутриклеточной воды, по-видимому, белкового происхождения. Поэтому при построении дальнейших рассуждений необходимо принять во внимание этот дополнительный фактор.
На рис. 20 представлена очень упрощенная схема процессов, происходящих на клеточной мембране. При рассмотрении схемы делается допущение, что мембрана непроницаема не только для высокомолекулярных анионов А-, но и для ионов Na+.
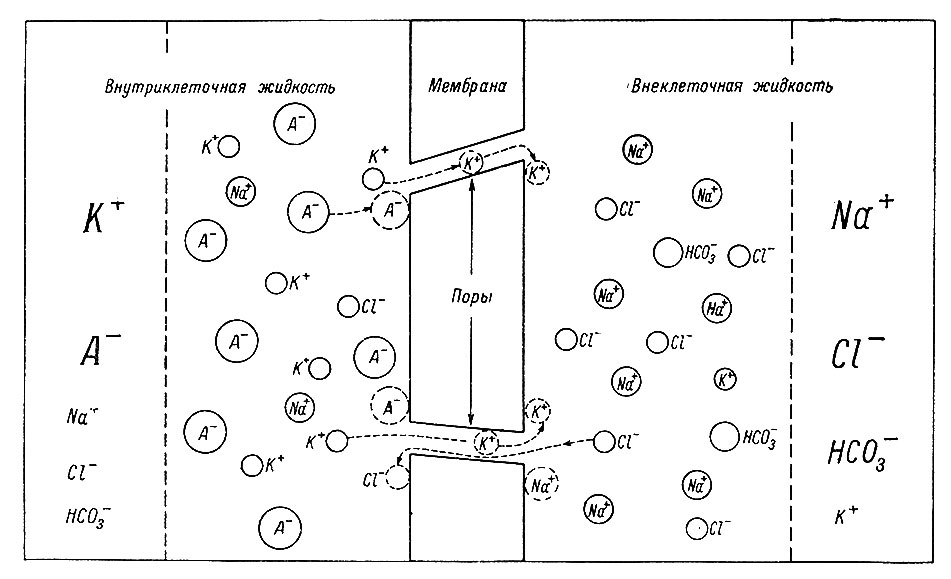
Рис. 20. Формирование трансмембранного потенциала под влиянием концентрационных градиентов. (Woodbury, 1963). Размеры символов в правой и левой колонках указывают на относительную концентрацию ионов во вне- и внутриклеточной жидкости. Пунктирные стрелки и кружки - направление движения ионов, К+, A-, Na+ и Сl- при перемещении К+ или Сl- через мембранные поры. Остальные объяснения в тексте
Пусть в какой-то исходный момент времени по обе стороны мембраны среда с растворенными в ней ионами электрически нейтральна, т. е. положительные и отрицательные частицы по обе стороны мембраны уравновешивают друг друга. Проследим поведение частиц, способных проникать через "мембранные поры".* Ввиду высокой внутриклеточной концентрации ионов К+ эти ионы будут диффундировать через клеточную мембрану изнутри кнаружи в соответствии с градиентом концентрации. Уравновешивающие электрический заряд ионов К+ высокомолекулярные анионы не могут их сопровождать ввиду того, что мембрана для них непроницаема. Ионы Na+ также не могут заменить их во внутриклеточной среде, так как, согласно допущению, они не проникают через мембрану снаружи внутрь. В результате возникает частичное разделение зарядов вокруг мембраны. Наружная ее сторона в результате появившегося избытка калия во внеклеточной среде начинает заряжаться положительно, а внутренняя сторона из-за появления не нейтрализованных калием высокомолекулярных ионов А- заряжается отрицательно. В районе мембраны возникает электрическое поле, которое начинает вмешиваться в происходящий процесс, поскольку диффундирующие ионы К+ имеют заряд. Как известно, одноименные электрические заряды отталкиваются, поэтому возникающий во внеклеточной среде положительный заряд начинает противодействовать дальнейшему поступлению ионов К+ изнутри клетки наружу. Таким образом, диффузия К+ из клетки наружу вызывает возникновение электростатических сил, препятствующих первичному диффузионному процессу, т. е. создается отрицательная обратная связь, ограничивающая выход К+ из клетки. Когда положительный потенциал внешней среды по отношению к соответственно нарастающему внутриклеточному отрицательному потенциалу достигает определенной величины, устанавливается динамическое равновесие между числом выходящим из клетки ионов К+ и числом этих ионов, входящих в клетку. Соответствующую этому моменту разность потенциалов по обе стороны мембраны обычно обозначают как потенциал равновесия для данного иона. Из хода рассуждений ясно, что его величина зависит от соотношений внутренней и наружной концентрации этого иона и может быть вычислена из уравнения Нернста.
* (Выражение "мембранные поры" не следует понимать буквально, как отверстия определенной величины. Неодинаковая проницаемость мембраны к различным частицам, по-видимому, связана со сложным взаимодействием между молекулами мембраны и этими частицами. Тем не менее размер проникающих частиц, как будет видно из дальнейшего изложения, играет существенную роль.)
Аналогичные рассуждения можно провести в отношении иона Сl-. Этот анион начинает поступать в условный исходный момент снаружи внутрь в связи с его относительно высокой концентрацией во внеклеточной жидкости. При этом внутри клетки создается отрицательный заряд, а на наружной поверхности мембраны - положительный. Как и в случае с К+, создается отрицательная обратная связь, в конце концов ограничивающая поступление ионов Сl- внутрь клетки по достижении потенциала равновесия между наружной и внутренней средой.
Естественно, что процесс выхода К+ из клетки и процесс вхождения в клетку ионов Сl- находится во взаимодействии и уровень устанавливающейся разности потенциалов определяется совокупностью происходящих событий.
На приведенной схеме не трудно разобраться в некоторых механизмах формирования МП покоящейся живой клетки.* Количественные расчеты с использованием уравнения Нернста показывают, что ионы Сl- и К+ распределяются по обе стороны мембраны приблизительно в соответствии с величиной МП, так что электрические и концентрационные градиенты уравновешивают друг друга.
* (Покоящейся условно называется клетка, не реализующая своей специфической деятельности. Как будет видно из дальнейшего, понятие покоя является физиологической абстракцией.)
Действительно описанный механизм возникновения МП мог бы иметь место, если бы мембрана клетки была полностью непроницаема для ионов Na+. Однако изящные и строгие исследования Ходжкина и Кейнса (Keynes, 1954; Hodgkin a. Keynes, 1955) с использованием радиоактивного изотопа натрия Na24 показали, что клеточная мембрана проницаема для Na+, хотя его проницаемость приблизительно в 50 раз ниже проницаемости для К+ и Сl-. На икроножной мышце лягушки экспериментально было показано (Keynes, 1954), что за секунду через 1 см2 клеточной поверхности внутрь мышечного волокна проникает около 10-11 M Na+. При таком "втекании" Na+ внутрь клетки без соответствующего "вытекания" из нее его внутриклеточная концентрация в течение часа должна была бы удвоиться. Однако этого на самом деле не происходит, хотя и концентрационный и электрический градиенты "понуждают" Na+ поступать внутрь клетки. Следовательно, должны существовать какие-то специальные механизмы, обеспечивающие прохождение ионов Na+ через мембрану против электрохимического градиента, т. е. изнутри наружу. Эти механизмы получили название активного переноса. Для осуществления последнего необходима постоянная затрата энергии, вырабатывающейся в результате клеточных метаболических процессов.
К сожалению, до сих пор остается невыясненным, каким образом энергия клеточного метаболизма используется при активном переносе, однако имеются достаточно четкие экспериментальные данные об участии в этом процессе аденозинтрифосфата и некоторых других фосфатов (Caldwell a. Keynes, 1957; Caldwell, Hodgkin, Keynes a. Shaw, 1960a; Hogdkin, 1964).
Прямую связь между активным переносом и обменом веществ впервые показали Ходжкин и Кейнс (Hodgkin a. Keynes, 1955) в своих исследованиях на гигантском аксоне каракатицы (sepia). Методика исследования основывалась на использовании радиоизотопа натрия - Na24 и позволила выявить ряд интересных закономерностей активного переноса. Прежде всего оказалось, что ингибиторы обмена веществ (динитрофенол, цианид, азид), блокирующие определенные звенья обменных окислительных реакций, почти полностью подавляют процесс выведения Na+ из клетки*. Аналогично действует снижение температуры препарата, резко уменьшающее уровень обменных процессов (рис. 21).
* (В последнее время показано также блокирующее действие азида на активный перенос ионов Na+ в мотонейронах спинного мозга кошек (Ito a. Oshima, 1964).)
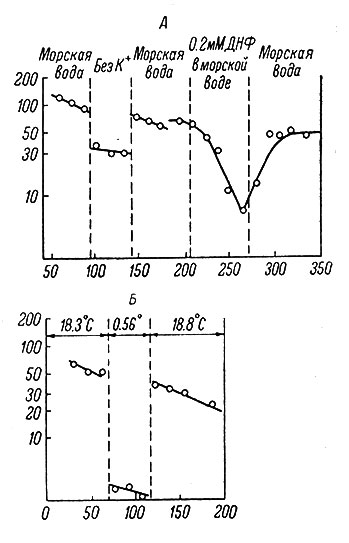
Рис. 21. Выход ионов Na+ из гигантского аксона (каракатицы) при изменении состава омывающего раствора добавлением динитрофенола (ДНФ) (А) и изменении температуры (Б) (Hodgkin a. Keynes, 1955). По оси абсцисс - время, в мин.; по оси ординат - выход радиоактивного Na24 из клетки, измеренный в импульсах в мин. Общий выход N+ (радиоактивного и обычного) пропорционален выходу радиоактивного Na+, исключая те изменения, которые возникают в результате постепенного разведения радиоактивного Na+ обычным ввиду естественных ионнообменных процессов (это постепенное падение концентрации радиоактивного Na+ показано в графе 'морская вода')
Далее было обнаружено, что выведение Na+ в общем пропорционально его внутренней концентрации и не зависит от его наружной концентрации. В то же время выход Na+ резко уменьшается при снижении концентрации калия во внешней среде и увеличивается при повышении внешней концентрации К+. Эта зависимость также показана на рис. 21. Кроме того, выяснилось, что метаболические яды снижают также поступление К+ из внешней среды внутрь аксона и что этот процесс блокируется указанными воздействиями почти в такой же степени, как выведение Na+ из клетки. Все это позволило сделать заключение, что механизм активного переноса работает по принципу электронейтральности, "вынося" ионы Na+ из клетки и "внося" в клетку эквивалентное количество ионов К+ (Hodgkin, 1958).*
* (Позднее было обнаружено, что связь между выведением Na+ и введением внутрь клетки К+ при активном переносе довольно свободная, во всяком случае не абсолютно жесткого типа (один к одному), как это предполагалось вначале (Caldwell, Hodgkin, Keynes a. Shaw, 1960a, 1960b). До последнего времени считалось, что активный перенос определяется уровнем внутренней концентрации Na+ (Hodkin a. Keynes, 1956; Hodgkin, 1958). В последних работах Экклса и его сотрудников приводятся данные о том, что калиевый компонент активного переноса активируется снижением внутренней концентрации К и что при этом внутрь клетки активно переносится КСl (Eccles, 1964; Eccles, Eccles a. Ito, 1964).)
Возникает вопрос, как может механизм, основанный на принципе электронейтральности, создавать поляризацию мембраны. Это не трудно понять, если учесть, что внутри клетки имеет место значительное количество высокомолекулярных анионов А- и что проницаемость ионов Na+ в 50 раз ниже проницаемости ионов К+. Будучи выведен из клетки механизмом активного переноса, натрий благодаря диффузии возвращается в клетку в 50 раз медленнее, чем введенный внутрь клетки калий выходит из нее в виде диффузионного потока. К тому же калий диффундирует из клетки в сопровождении нейтрализующего его иона Сl-. В результате перечисленных процессов абсолютное количество положительных ионов внутри клетки убывает: активно выводится Na+ и пассивно - сопровождаемый ионами Сl- калий. В клетке возникает избыток отрицательных зарядов благодаря наличию высокомолекулярных ионов А-.
Это, конечно, весьма упрощенная система рассуждений. Тем не менее она в общих чертах отражает существо явлений, не касаясь некоторых усложняющих деталей, например, вопроса о распределении в этих условиях воды.
Существует много различных гипотез, в которых делается попытка объяснить механизм активного переноса, однако ни одна из них не доказана экспериментально. Наиболее привлекательны схемы с так называемым "промежуточным носителем". В качестве примера можно привести схему Шоу-Глинна (Glynn, 1957) (рис. 22) Преимущество такой схемы заключается в том, что она не предполагает жесткой связи между выведением Na+ и поступлением в клетку К+. Так, сохранение частичного выведения Na+ при полном отсутствии К+ во внешней среде может быть объяснено тем, что Na+ имеет также некоторое сродство и к субстанции х. Гипотетическая схема должна объяснять такую возможность, поскольку выведение Na+ действительно частично сохраняется даже при полном отсутствии К+ во внеклеточной среде.
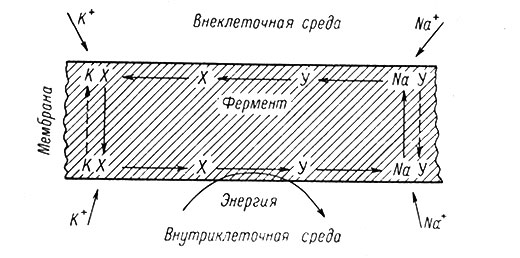
Рис. 22. Гипотетическая схема калий-натриевого обменного 'насоса'. (Glynn, 1957). Предполагается, что субстанции X и Y функционируют внутри мембраны. X обладает большим сродством к К+; Y обладает большим сродством к Na+. X и У перемещаются через мембрану только в комбинации с соответствующим ионом
До сих пор все явления и механизмы, связанные с генерацией МП, в целях простоты изложения описывались лишь с качественной стороны. Однако для более ясного представления о происходящих процессах целесообразно привести некоторые количественные характеристики поляризации мембраны, тем более что это позволит также составить более четкое представление об объеме происходящих ионообменных процессов.*
* (Нижеследующий цифровой материал взят из "Нейрофизиологии" Т. Ру и соавторов (Ruch et al., 1963).)
Емкость мембраны поперечнополосатого мышечного волокна лягушки определена в эксперименте и составляет около 10 мкф на см2. Величина заряда мембраны - этого биологического конденсатора - определяется величиной разности потенциалов по обе стороны мембраны (Ем) и ее емкостью (См): q = Cм ⋅ Ем. Ем примем за 90 мв. Тогда заряд q = 10 × 10-6 ф/см2 × 0.09 в = 9 × 10-7 кулонов на 1 см2. Если пересчитать полученную величину заряда на число ионов, участвующих в его формировании, то получаются следующие результаты.
По закону Авогадро 1 граммолекула содержит 6.023 × 1023 молекул. В данном случае мы имеем дело с одновалентными ионами, несущими на себе 1 ед. заряда, равную по величине заряду одного электрона. Заряд электрона, выраженный в кулонах, составляет 1.6 × 10-19. Тогда заряд одного моля одновалентных катионов составляет 1.6 × 10-19 × 6.023 × 1023 = 96500 кулонов. Поскольку заряд на клеточной мембране мышечного волокна составляет 9 × 10-7 кулонов см2, то это означает, что эта мембрана на участке 1 см2 разделяет всего 9 × 10-7/96500 = 9.5 × 10-12 моля ионизированных одновалентных частиц. В то же время в 1 см3 внутриклеточной жидкости содержится 1.5 × 10-6 моля катионов или анионов, т. е. в несколько миллионов раз больше. Подсчеты показывают, что слой внутриклеточной жидкости толщиной всего в 6 Å обеспечивает достаточное количество ионов, чтобы создать на мембране потенциал в 90 мв.
Эти величины поясняют, какое незначительное количество ионов от их общего числа в клетке принимает участие в поддержании МП и, как это будет показано ниже, в генерации потенциала действия.
Следует также отметить, что клетка располагает достаточными энергетическими возможностями для осуществления активного переноса Na+. Кейнс и Майзель (Keynes a. Maisel, 1954) экспериментально показали, что расход энергии на активный перенос Na+ в скелетной мышце лягушки значительно меньше общих энергетических расходов клетки, рассчитанных по потреблению кислорода.* В большинстве опытов в покоящейся мышце только около 10% энергетических расходов идет на активное выведение Na+. Если принять, что коэффициент полезного действия при активном переносе составляет только 50% или даже меньше, то все равно энергетический расход на этот процесс образует относительно небольшую часть энергии, вырабатываемой клеткой. Эти количественные данные существенно подкрепляют концепцию механизма активного переноса, показывая, что с точки зрения энергетического баланса клетки подобный процесс вполне возможен.
* (В целях упрощения изложения формула расчета мощности, затрачиваемой на активный перенос Na+, не приводится. В принципе эта мощность является произведением электрохимического потенциала для Na+ с отрицательным знаком (-ENa) на величину выходящего потока ионов натрия (Пвых.Na))
ПОИСК:
© ANFIZ.RU, 2011-2022
При использовании материалов сайта активная ссылка обязательна:
http://anfiz.ru/ 'Анатомия и физиология человека'
При использовании материалов сайта активная ссылка обязательна:
http://anfiz.ru/ 'Анатомия и физиология человека'