Занятие 21. Лейкоцитозы и лейкопении
Цель занятия
Изучить количественные и качественные изменения лейкоцитов при некоторых патологических состояниях.
Подготовка к занятию
Студенты готовятся к данному занятию в объеме следующих вопросов.
1. Лейкоцитозы и лейкопении: физиологические и патологические, перераспределительные и истинные. Рефлекторная и нервно-эндокринная регуляция лейкоцитарных реакций.
2. Лейкоцитозы: нейтрофильный, эозинофильный, лимфоцитарный и моноцитарный, их связь с определенными нозологическими формами и природой патологического процесса. Понятие о ядерных сдвигах. Индекс ядерного сдвига.
3. Лейкоцитарная формула как показатель функционального состояния системы крови. Понятие об относительном и абсолютном увеличении или уменьшении отдельных форм лейкоцитов.
Техническое оснащение занятия*
* (На группу в 10-12 человек.)

Наименование опытов и методика их проведения
Опыт 1. Изменение характера лейкоцитарной реакции на внутрибрюшинное введение молока у кролика на фоне действия новокаина. В опыт берут 2 кроликов одинакового веса.
Одному из них вводят внутрибрюшинно смесь 5 мл охлажденного кипяченого молока с 5 мл физиологического раствора.
Другому - смесь 5 мл молока с 5 мл 1% раствора новокаина. Количество лейкоцитов в периферической крови исследуют до опыта и трижды с интервалами в 30 минут после введения молока.
В протокольных тетрадях студенты вычерчивают лейкоцитарные кривые, полученные у контрольного и подопытного кроликов, и делают заключение о предполагаемом механизме изменения лейкоцитарной реакции у подопытного кролика.
Методика определения количества лейкоцитов (безмеланжерный способ)
Из прокола краевой вены предварительно обработанного эфиром уха кролика набирают 0,02 мл крови в гемометрическую пипетку и выдувают на дно пробирки, в которую заранее отмерено 0,38 мл 3% раствора уксусной кислоты. Пипетку трижды промывают. Смесь энергично встряхивают в течение 3 минут. Пипеткой для дистиллированной воды от гемометра каплю смеси вносят в счетную камеру. Лейкоциты подсчитывают в 100 больших квадратах сетки Горяева.
Количество лейкоцитов в 1 мм3 крови вычисляют по формуле:
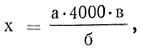
где х - искомое количество лейкоцитов;
а - сумма лейкоцитов, сосчитанных в 100 больших квадратах;
б - количество сосчитанных малых квадратов (1 большой квадрат равен 16 малым);
в - разведение крови (в 20 раз).
Объем малого квадрата равен 1/4000 мм3 (1 сторона - 1/20 мм; высота - 1/10 мм. Объем равен 1/20×1/20×1/10 = 1/4000 мм3). Поэтому для приведения к 1 мм3 формула содержит множитель 4000.
Пример. В 100 больших (1600 малых) квадратах сосчитано 150 лейкоцитов.
В 1 мм3 будет:
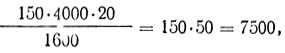
т. е. сумму лейкоцитов, сосчитанных в 100 больших квадратах, нужно умножить на 50.
Приготовление смеси лейкоцитов для их подсчета можно проводить также обычным (меланжерным) способом. Кровь набирают до метки 0,5, разводящую жидкость - до метки 11, нанесенной на лейкоцитарном меланжере (разведение в 20 раз). В дальнейшем поступают так же, как при обращении с эритроцитарным смесителем.
Опыт 2. Экспериментальная пострадиационная лейкопения у крыс. За 5 суток до занятия крысу подвергают общему рентгеновскому облучению в дозе 600 г. Одним из непременных признаков возникновения лучевой болезни на определенной ее стадии является резкое падение количества лейкоцитов в крови.
На занятии демонстрируются также внешние признаки лучевого синдрома у крыс. Обращают внимание на геморрагии у глаз, носа, изменение шерстного покрова, диарею, похудание, изменение общего поведения (вялость).
Для подсчета лейкоцитов в крови у облученной крысы используется, как и в опыте 1, безмеланжерный способ.
Техника взятия крови у крыс
Крысу помещают в камеру. После обработки спиртом корня хвоста производят надрез скальпелем или бритвой одной из его боковых сторон над просвечивающей веной на глубину 1-2 мм. Первую каплю крови вытирают, вторую набирают до метки в мерную пипетку от гемометра. Дальнейший ход определения тот же, что и в опыте 1. При повторных взятиях крови надрезы производят на расстоянии 1-1,5 см от предыдущих по направлению к концу хвоста.
Изучение демонстрационных препаратов (мазков) крови
1. В мазках, выставленных под микроскопом к началу занятия, студенты изучают и зарисовывают нормальные и патологические формы лейкоцитов (нейтрофилы: сегментоядерные, палочкоядерные, юные, миелоциты; эозинофилы, базофилы, лимфоциты, моноциты, клетки раздражения, дегенеративные формы нейтрофилов с дегенеративными ядрами и токсогенной зернистостью в протоплазме).
2. Студенты получают от преподавателя по одному пронумерованному мазку с указанием числа лейкоцитов в 1 мм3 крови. Подсчитывают лейкоцитарную формулу и проверяют ее правильность по списку формул, находящемуся у преподавателя. После этого студенты делают заключение об изменении абсолютных количеств отдельных форм лейкоцитов и об особенностях лейкоцитарного сдвига.
ПОИСК:
© ANFIZ.RU, 2011-2022
При использовании материалов сайта активная ссылка обязательна:
http://anfiz.ru/ 'Анатомия и физиология человека'
При использовании материалов сайта активная ссылка обязательна:
http://anfiz.ru/ 'Анатомия и физиология человека'