Нарушения белкового обмена
Нарушения белкового обмена сопровождают самые разнообразные заболевания и имеют место на разных его этапах.
Нарушение переваривания и всасывания белков возникает при различных расстройствах секреторной функции желудочно-кишечного тракта, сопровождающихся расстройствами пищеварения.
При этом могут быть нарушены процессы переваривания белков в том или другом отделе желудочно-кишечного тракта и всасывания продуктов их ферментативного распада.
При расстройствах функции кишечника развиваются процессы усиленного гниения, сопровождающиеся повышенным дезаминированием и декарбоксилированием аминокислот с образованием индола, скатола, фенола, крезола, кадаверина, путресцина, а также образованием продуктов неполного распада белков.
Нарушения межуточного белкового обмена
В межуточном белковом обмене наблюдаются разнообразные нарушения. Распад белков под влиянием протеиназ вызывает накопление полипептидов, некоторые из которых обладают физиологической активностью. В результате нарушения межуточного белкового обмена могут наступить явления интоксикации, например при хрониосепсисе, обширных травматических и воспалительных поражениях, раневом истощении. Расстройства межуточного белкового обмена возникают также в связи со сложными и многообразными процессами декарбоксилирования, дезаминирования, переаминирования, синтеза аминокислот, в которых принимают участие разные органы, особенно печень.
Усиление декарбоксилирования в тканях ведет к накоплению протеиногенных аминов, которые обладают значительной физиологической активностью, например гистамина, образующегося из гистидина, тирамина - из тирозина. Это имеет место при ожоге, местной анемии тканей, некробиозе, аллергических процессах.
Нарушение окислительного дезаминирования встречается вследствие недостаточного поступления в организм витамина С. При этом нарушается окисление тирозина и фенилаланина и усиленное выведение их с мочой. Недостаточное поступление витамина B1 нарушает ферментативные системы переаминирования, дезаминирования и аминирования и сопровождается нарушением мочевинообразования и повышенным выделением аминокислот. Авитаминоз В6 характеризуется ослаблением процессов декарбоксилирования и переаминирования, а также понижением обмена триптофана, что влечет за собой нарушение синтеза белка и усиленное выделение с мочой продуктов триптофанового обмена - кинуреновой и ксантуреновой кислот. Аминокислотный обмен изменяется и при недостатке других витаминов комплекса В.
Известны также прирожденные изолированные нарушения промежуточного аминокислотного обмена, развивающиеся в результате ферментативной недостаточности.
К ним относятся, например, такие аномалии белкового обмена, как фенилпиро- виноградная олигофрения (фенилкетонурия), алкаптонурия и др. Первое заболевание характеризуется тем, что ввиду отсутствия соответствующего фермента фенил- аланин не может превратиться в оксифенилаланин, накапливается в организме и обусловливает развитие слабоумия. При алкаптонурии ввиду отсутствия гомогентизиназы образующаяся из тирозина гомогентизиновая кислота не окисляется и выделяется с мочой. При длительном течении этого заболевания развиваются патологические изменения в суставах и пороки сердечных клапанов. От пропитывания тканей гомогентизиновой кислотой появляется сине-черная окраска (охроноз) на покровах лица, склерах, ногтях, в стенках сосудов и хрящах.
Цистиноз характеризуется отложением цистина в органах и тканях. В его основе лежит первичное расстройство цистин-цистеинового обмена. Отложение цистина в почках может вызвать вторичное тяжелое нарушение в виде ограничения реабсорбции в канальцах, вследствие чего цистин, а нередко и другие аминокислоты выделяются в увеличенном количестве с мочой.
О расстройствах промежуточного белкового обмена судят также по увеличению или уменьшению содержания азота в крови и моче, а также по изменению соотношения между различными фракциями белка и азотистых продуктов белкового обмена. Так, при нарушениях белкового обмена нередко изменяется соотношение между отдельными фракциями белка в крови, увеличение количества остаточного азота, уменьшение коэффициента общего азота к остаточному. Одним из важных показателей нарушения белков в крови является изменение глобулино-альбуминового коэффициента.
Гипопротеинемия - понижение содержания белков в крови - обычно характеризуется понижением содержания альбуминов, например при заболеваниях почек, качественном голодании или кахексии. Гиперпротеинемия - увеличение белков в крови - касается преимущественно увеличения содержания глобулинов. Повышение γ-глобулинов связано с развитием специфического иммунитета - образованием антител.
В крови может также изменяться содержание белковых компонентов, входящих в состав свертывающей системы крови.
При некоторых формах почечных заболеваний в крови увеличивается содержание остаточного азота - ретенционная гиперазотемия. Тяжелая недостаточность печени также сопровождается увеличением в крови содержания остаточного азота - продукционная гиперазотемия. В моче нарастание азота - гиперазотурия - происходит преимущественно за счет аммонийных солей. Повышение содержания аммиака в моче имеет место вследствие ослабления способности печени синтезировать мочевину. Возможно также, что увеличенное выведение аммиака при недостаточности печени объясняется нейтрализацией им накапливающихся кислых продуктов обмена и выведением их с мочой.
Общие нарушения белкового обмена
Общие нарушения белкового обмена характеризуются изменением азотистого баланса, который становится отрицательным. Такие нарушения чаще всего наблюдаются при голодании, инфекциях и интоксикациях.
Белковый обмен значительно нарушен при инфекционных процессах, когда повышаются основной обмен и специфико-динамическое действие белков, а также возникает токсогенный распад белка.
Разнообразные отравления также характеризуются отрицательным азотистым балансом. В крови обнаруживается повышение содержания остаточного азота. Такие явления наблюдаются при отравлениях окисью углерода, лизолом, сулемой.
Обычно яды, ведущие к глубоким изменениям печени, одновременно вызывают нарушение белкового обмена. Отравление фосфором, мышьяком или сурьмой ведет к нарастанию количества остаточного азота в крови и к усиленному выделению азота с мочой.
Нарушения в белковом обмене развиваются также при злокачественных опухолях, болезнях почек, крови и кровотворных органов. Повышение белкового обмена имеет место при некоторых эндокринных заболеваниях, особенно при базедовой болезни и паратиреоидной тетании, а также при усилении функции коры надпочечников.
Нарушение креатинового и креатининового обмена
Появление креатина в моче, в которой обычно его не обнаруживают, свидетельствует о нарушении креатинового обмена. Креатинурия наблюдается при голодании, недостаточности углеводов в пище, особенно при истощении в мышцах запаса гликогена, например при мышечных дистрофиях, тетании, адинамии от недостаточности коры надпочечников, выраженных кахексиях, нарушении иннервации мышц. Во всех указанных случаях важное значение имеет нарушение обмена в мышцах, где креатин играет существенную роль, входя в состав фосфагена.
То обстоятельство, что креатинурия наблюдается при недостатке углеводов в пище, указывает на связь между углеводным и креатиновым обменом в мышцах. О том же говорят исследования так называемого креатининового коэффициента, т. е. суточного количества креатининового азота мочи, перечисленного на 1 кг веса. Этот коэффициент ниже у женщин и детей, по-видимому, вследствие более слабого развития мускулатуры и относительно более низкого в ней обмена углеводов. Он увеличивается при усиленной мышечной деятельности (при охлаждении, тренировке и пр.).
Появление креатина в моче наблюдается также при некоторых нарушениях функции почек. При креатинурии в большинстве случаев одновременно уменьшается выведение креатинина вследствие замедленного перехода образующегося креатина в креатинин.
Нарушения нуклеопротеидного обмена
Под патологией нуклеопротеидного обмена следует понимать нарушение обмена сложных белковых тел, состоящих из белка и нуклеиновых кислот и входящих главным образом в состав ядерного вещества тканей.
Нуклеопротеиды являются источником образования мочевой кислоты. При кормлении беспуриновой пищей количество мочевой кислоты в крови колеблется от 2 до 3 мг% (так называемая эндогенная мочевая кислота, образующаяся как продукт тканевого обмена). В зависимости от количества экзогенно вводимых пуринов содержание мочевой кислоты в крови может нарастать. Содержание мочевой кислоты в суточном количестве мочи колеблется в пределах от 0,6 до 1,2 г.
Усиленное образование мочевой кислоты и накопление ее в крови наблюдаются не только от увеличенного поступления в организм нуклеиновых веществ извне (мясная пища, кормление печенью и зобной железой), но и вследствие патологических разрушений клеток, например при пневмонии, лейкемии, злокачественных новообразованиях, лихорадке.
Причиной накопления мочевой кислоты в крови может быть нарушение выделительной способности почек.
Выяснение путей пуринового обмена и образования мочевой кислоты в организме приобретает особенно большое значение в связи с тем изменением пуринового баланса, которое лежит в основе подагры.
Подагра1 характеризуется проявляющимся в виде приступов воспалением, суставов. При ней происходит значительное накопление мочевой кислоты в виде мочекислого натрия и выпадение ее в кристаллическом виде преимущественно в мезенхимной ткани - хрящах, суставных сумках, сухожилиях, фасциях, а также в мышцах, коже и даже в почках. При этом нередко наблюдается образование узлов (tophi urici) (рис. 40).
1(От греческих слов: pous - нога и agrios - жестокий.)
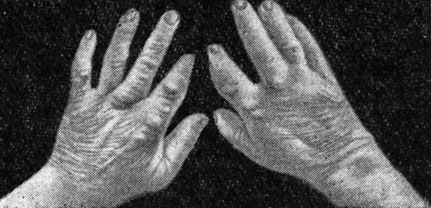
Рис. 40. Arthritis urica. Множественные подагрические узлы на руках
Количество мочевой кислоты в крови обычно бывает повышено перед приступом (10 - 15 мг% и выше). Приступ характеризуется острой болью в пораженном суставе (преимущественно в большом пальце ноги).
Выведение мочевой кислоты у больных подагрой в отличие от других случаев накопления ее в крови замедлено, что особенно заметно при искусственном введении ее в организм. Подагра наряду с высокой концентрацией мочевой кислоты в крови характеризуется низкой концентрацией ее в моче. Во время приступа и непосредственно вслед за ним количество выводимой с мочой мочевой кислоты резко повышается и затем снова падает.
Важными патогенетическими факторами возникновения подагры считают повышение эндогенного образования мочевой кислоты и задержку ее в организме вследствие функционального изменения почек, которое влечет за собой уменьшение выделения мочевой кислоты, в результате чего происходит ее накопление в крови и отложение в тканях (гиперурикемия). Действительно, выведение мочевой кислоты при подагре заметно падает.
Полагают, что при этом наибольшее значение имеет нарушение иннервации почек. Опытами было установлено, что возбуждение симпатических нервов усиливает, а их торможение уменьшает выведение мочевой кислоты почками.
Сущность функциональных нарушений, ведущих к развитию подагрического приступа, усматривается в развитии аллергического состояния организма. Сторонники этого взгляда сближают подагру с аллергическими заболеваниями. Как и подагра, эти болезни также проявляются приступами. При них часто обнаруживаются нарушения в обмена пуринов.
Отложение уратов именно в хрящах, сухожилиях и слизистых сумках, очевидно, объясняется физико-химическими особенностями этих тканей. Хрящи и сухожилия богаты натриевыми ионами, что, вероятно, отражается на растворимости мочекислого натрия в суставах и сухожилиях. Наряду с этим выпадению мочекислого натрия в суставах и сухожилиях способствует чрезвычайно медленная циркуляция тканевой жидкости в этих органах, развитие в них гипоксии и ацидоза.
Развитию подагры очень способствует богатая нуклеинами пища, алкоголь, свинцовые отравления, вероятно, потому, что все эти вещества отягощают нуклеиновый обмен и функцию почек.
ПОИСК:
© ANFIZ.RU, 2011-2022
При использовании материалов сайта активная ссылка обязательна:
http://anfiz.ru/ 'Анатомия и физиология человека'
При использовании материалов сайта активная ссылка обязательна:
http://anfiz.ru/ 'Анатомия и физиология человека'