Нарушения обмена липидов
Нарушения жирового обмена
Жиры, вводимые в организм, подвергаются перевариванию панкреатическим и кишечным соком. Они всасываются через стенку тонких кишок. Уже в самой стенке происходит ресинтез жиров из жирных кислот и глицерина. Некоторое количество нейтральных жиров может всосаться, не расщепляясь на жирные кислоты и глицерин. Как показали исследования с изотопами, жир всасывается главным образом через лимфатическую систему и лишь отчасти (не более 30%) через систему воротной вены. Всосавшись, основная масса жиров откладывается в жировых депо - подкожной жировой клетчатке, сальнике, брыжейке, жировых прослойках органов. Синтез жиров из углеводов и белков совершается в печени, молочной железе (при лактации), а также в самой жировой ткани. Жиры из жировых депо транспортируются в органы, преимущественно в печень, где подвергаются окислению, особенно в тех случаях, когда истощаются запасы углеводов, например гликогена в печени.
Регуляция транспорта жира осуществляется нервной системой. Обеднение печени гликогеном вызывает раздражение ее интерорецепторов, передающих импульсы в центральную нервную систему. Оттуда по эфферентным путям симпатической нервной системы через спинной мозг импульсы поступают в жировую ткань, происходит мобилизация жира из жировых депо. Высокая перерезка спинного мозга блокирует мобилизацию жира, ускоряет исчезновение из печени жира, ранее накопившегося вследствие обеднения ее гликогеном. По некоторым данным, центральная зона регуляции жирового обмена находится в гипоталамической области.
Эндокринные железы влияют на жировой обмен (главным образом гормоны щитовидной железы, инсулин, соматотропный гормон передней доли гипофиза, глюкокортикоиды коры надпочечников и половые железы). Эти гормоны, кроме инсулина, повышают жировой обмен, тогда как инсулин усиливает превращение углеводов в жир.
Нарушение всасывания и отложения жира
Переваривание и всасывание жира могут быть нарушены в связи с различными изменениями: 1) расстройством внешней секреции поджелудочной железы, непоступлением в двенадцатиперстную кишку липазы, необходимой для расщепления жира; 2) значительным понижением или полным отсутствием выделения желчи, необходимой для эмульгирования жира; 3) усилением перистальтики, вследствие чего жир не успевает всосаться; 4) понижением способности эпителия слизистой оболочки кишечника активно воспринимать жир.
Расстройства переваривания и всасывания жира наблюдаются при энтеритах, гиповитаминозах, недостаточности ресинтеза триглицеридов вследствие нарушения функции коры надпочечников.
Наличие в кале 20% введенного с пищей жира (вместо 5 - 10% в норме) считается патологическим явлением.
Накопление жира в клетках, не относящихся к жировой ткани, в необычном количестве или необычного химического состава носит название жировой дистрофии. В основе жировой дистрофии лежит повреждение клетки, нарушение в ней метаболизма. Жировая дистрофия встречается преимущественно в печени, миокарде и почках.
Жир, обнаруживаемый в клетке при жировой дистрофии, может быть результатом поступления и задержки жира, принесенного в клетку лимфой или кровью, - жировая инфильтрация. Возможно также проявление жира в клетках вследствие нарушения физико-химических и биохимических процессов в самой протоплазме - жировой фанероз. Установить происхождение жира в клетке при ее повреждении практически часто представляется очень затруднительным.
Химический состав жировых веществ при жировой дистрофии может быть различным. Наряду с нейтральным жиром возможно отложение фосфатидов, свободного и связанного холестерина (анизотропное ожирение).
Накопление жира в клетках (например, печеночных) вызывают разные патогенетические факторы: 1) нарушение расщепления жира и окисления высших жирных кислот при воздействии таких ядов, как четыреххлористый углерод, фосфор, хлороформ, бактериальные токсины; 2) недостаточная доставка тканям или недостаточное использование ими кислорода (гипоксия), например при злокачественной анемии, некоторых авитаминозах; 3) нарушение выхода жира из ткани из-за расстройства обмена фосфолипидов, обеспечивающих тонкое диспергирование жира, например при отсутствии в пище холина, метионина и других липотропных веществ либо при поступлении в организм веществ, тормозящих синтез холина, например гуанидиноуксусной кислоты, которая своей метильной группой усиливает синтез креатина и тем самым тормозит синтез холина.
Механизм липотропного действия холина заключается в том, что он принимает участие в синтезе фосфолипидов и таким образом активизирует выход жира из печени. Метионин же участвует в образовании холина при помощи отщепления своей метильной группы. Поэтому наступление жировой инфильтрации печени можно предотвратить введением холина и метионина, содержащегося в казеине, белках судака, трески и некоторых других продуктах питания.
Гиперлипемия
Повышение содержания нейтрального жира в крови (более 200 мг%) носит название гиперлипемии. Различают: 1) пищевую, или алиментарную, гиперлипемию (от введения с пищей большого количества жира), которая достигает максимума обычно через 3 - 4 часа после приема пищи и исчезает через 6 - 9 часов; 2) транспортную гиперлипемию при патологических состояниях, которые сопровождаются мобилизацией жира из жировых депо вследствие обеднения печени гликогеном, например при голодании, сильных интоксикациях, тяжелом диабете; 3) ретенционную гиперлипемию от замедления поступления жира из крови в ткань вследствие нарушения комплексов жира с белками плазмы, например при геморрагической анемии, застойной желтухе, диабете, нефрозе и некоторых других заболеваниях.
Нарушения межуточного жирового обмена
Одним из проявлений расстройства межуточного жирового обмена является увеличение содержания кетоновых тел (β-оксимасляной и ацетоуксусной кислот, ацетона) в крови - кетонемия и выделение их с мочой - кетонурия.
Кетоновые тела в основном образуются в печени и окисляются в других тканях до углекислоты и воды. Истощение гликогенных резервов печени сопровождается накоплением жира в этом органе и повышенным кетонообразованием, например при голодании и диабете. Кетоз, т. е. накопление кетоновых тел в организме, наблюдается также при недостаточном ресинтезе кетоновых тел в высшие жирные кислоты или нарушении их окисления в трикарбоновом цикле. Обеднение печени гликогеном и кетонемия могут возникать в связи с односторонним питанием жирами, голодании, недостаточностью углеводов в пище или недостаточным использованием их, например при диабете.
Вследствие недостатка углеводов жир в увеличенном количестве идет на покрытие дефицита в энергии и в печени кетонов образуется больше, чем их могут использовать ткани. Введение в организм углеводов уменьшает поступление жира в печень и тем самым может предупредить или устранить развитие кетонемии.
Ожирение
Ожирение - это патологическое отложение жира в жировых депо, причем вес тела (особенно при общем ожирении) значительно возрастает и может доходить до 190 кг и более.
Причины ожирения следующие: 1) нарушение питания, выражающееся в повышении поступления в организм пищи при относительно меньшем расходовании энергии, т. е. нарушение энергетического баланса; 2) недостаточное потребление жировых запасов и вследствие этого увеличенное их образование и отложение в условиях нормального питания; 3) сочетание обоих факторов.
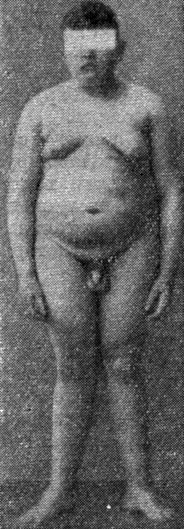
Рис. 35. Церебральное ожирение у 14-летнего мальчика после перенесенного энцефалита
В первом случае большое значение имеет повышение аппетита вследствие кортикальных влияний, установившихся благодаря привычке, воспитанию, а также в связи с унаследованным или приобретенным нарушением функции диэицефальной области, регулирующей чувство аппетита, например после перенесенного энцефалита, при опухолях или травме гипоталамуса (так называемое гипоталамическое ожирение) (рис. 35 и 36).
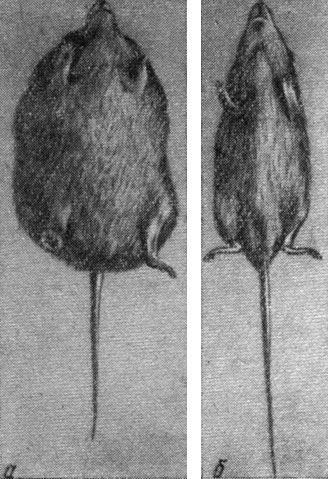
Рис. 36. Экспериментальное гипоталамическое ожирение. а - крыса, у которой вызвано гипотала- мическое ожирение; возраст 493 дня, вес 897 г; повреждение гипоталамуса произведено в возрасте 39 дней; б - контрольное животное в возрасте 493 дней; вес 290 г
Недостаточное потребление жира может быть результатом нарушения нейро-эндокринной и эндокринной регуляции. Сюда относятся:
1. Ожирение вследствие нарушения функции центральных вегетативных образований, поражение области межуточного мозга, нередко в сочетании с понижением функции передней доли гипофиза и половых желез (адипозо-генитальная дистрофия). Такое ожирение характеризуется отложением жира преимущественно в области ягодиц, бедер, грудных желез, на спине и в нижнем отделе живота; в виду понижения функции передней доли гипофиза отмечается также задержка роста и отставание полового развития (рис. 37).
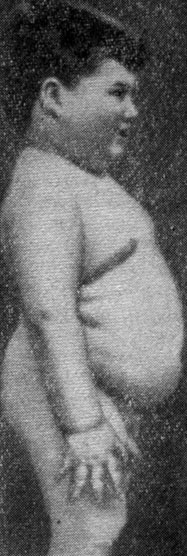
Рис. 37. Гипофизарное ожирение у мальчика
2. Гипофизарное ожирение - болезнь Иценко-Кушинга, которая имеет в основе своего возникновения повышение функции передней доли гипофиза и увеличение продукции адрено-кортикотропного гормона, активизирующего выделение глюкокортикоидов корой надпочечников. Благодаря этому усиливается отложение жира на туловище, лице и затылке.
3. Ожирение, наблюдаемое при синдроме Кушинга, который характеризуется первичным усилением продукции глюкокортикоидов, например при опухоли корковой части одного из надпочечников.
4. Гипотиреоидное ожирение с равномерным расположением жира на туловище и конечностях.
5. Гипогенитальное ожирение, например у кастратов с отложением жира в области ягодиц, живота, груди и внутренйей стороны бедер (рис. 38).
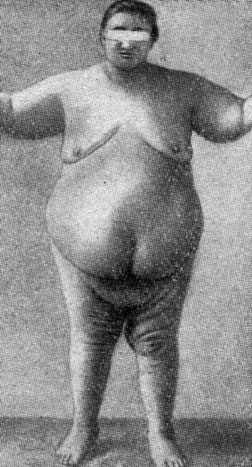
Рис. 38. Гипогенитальное ожирение у 67-летней женщины
6. Инсулярное ожирение - от повышенной продукции инсулина, усиливающего переход углеводов в жир и угнетающего мобилизацию жира.
Встречаются также регионарные отложения жира (рис. 39). Они возникают на почве повреждения вегетативных нервов - выпадения симпатических или раздражения парасимпатических, тогда как раздражение симпатической нервной системы может сопровождаться уменьшением жировых депо и даже истощением. В происхождении регионарных отложений жира, по-видимому, имеет значение и свойство подкожной клетчатки накапливать жир (так называемая тканевая липофилия).
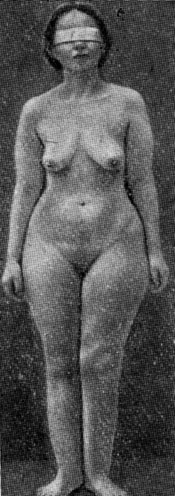
Рис. 39. Регионарное ожирение нижней части тела
Происхождение эндокринных форм ожирения не следует представлять себе как результат нарушения функции только одной из желез внутренней секреции. В большинстве случаев ожирение развивается в результате сочетания нарушений центральной нервной системы и функции нескольких эндокринных желез с преимущественным нарушением одной из них.
В возникновении ожирения большую роль играют и другие, дополнительные факторы. Среди них следует указать на отсутствие достаточных движений, например при ослаблении мышечной работы, особенно при параличах и парезах, при уже развившемся ожирении или при болезнях сердца.
Способствуют ожирению хронические интоксикации (например, алкоголем), в результате чего, с одной стороны, понижаются тканевые окислительные процессы, с другой - увеличивается освобождение энергии в организме за счет сгорания алкоголя.
Исхудание
Исхудание возникает от следующих основных причин:
1) недостаточное по сравнению с энергетическим расходованием поступление пищи либо отсутствие аппетита на почве расстройства деятельности нервной системы, инфекции и интоксикации;
2) нарушение усвоения жира или усиление потери жира. Нарушение усвоения жира может быть результатом недостаточного всасывания его в кишечнике при частых рвотах, расстройствах желудочно-кишечного пищеварения , авитаминозах, интоксикациях;
3) расстройства регуляторных функций. Среди них, кроме расстройств функции центральной нервной системы, например некоторых поражений диэнцефальной области, регулирующей обмен веществ, следует назвать перевозбуждение симпатической нервной системы на почве длительных болевых ощущений, переутомления, тиреотоксикоза;
4) расстройства эндокринных функций, как это, например, имеет место при гипофизарной кахексии и сахарном диабете.
Нарушения фосфолипидного обмена
Фосфолипиды, в основном лецитины и кефалины, являются важной составной частью клеток (особенно мозговых), где они включаются в белково-липоидные комплексы. Сходство в растворимости и нередко общее местонахождение липоидов и жиров как в нормальных, так и в патологических условиях позволяют установить связь нарушений липоидного обмена с жировым, хотя по химическим и физиологическим свойствам липоиды отличны от жиров.
Фосфолипиды, главным образом лецитины, участвуют в обмене жира. Содержащиеся в них жирные кислоты легко выводятся из клеток. На этом основано действие липотропных веществ, участвующих в образовании фосфолипидов.
Повышенное содержание лецитина в крови нередко наблюдается наряду с увеличением в ней жира. Изменение содержания лецитина в крови чаще всего имеет место в связи с нарушениями жирового обмена и функции кровотворных органов.
При тканевых дистрофиях фосфолипиды легко распадаются и освобождают высшие жирные кислоты, которые идут на построение сложных эфиров холестерина.
Известны некоторые патологические состояния, связанные с отложением фосфолипидов - цереброзидов. Так, при болезни Гоше цереброзиды откладываются в макрофагальных клетках селезенки, печени, лимфатических узлов и костного мозга. При некоторых других патологических состояниях в клетках происходит отложение сфингомиелина и лецитина, например при спленомегалии (болезнь Нимана-Пика у детей).
Нарушения холестеринового обмена
Увеличение содержания холестерина в крови (выше 180 - 200 мг%) - гиперхолестеринемия - может быть различного происхождения: 1) экзогенная, или алиментарная, гиперхолестеринемия вследствие усиленного поступления холестерина с пищей - желтками яиц, маслом, печенкой; 2) эндогенная гиперхолестеринемия, имеющая в основе своего возникновения: а) повышение синтеза холестерина или мобилизацию его из тканей, например при клеточном распаде, заболеваниях печени, диабете, б) недостаточное выведение холестерина желчью или кишечником, например при застойной желтухе и хронических заболеваниях печени (ретенционная гиперхолестеринемия), в) нарушение транспорта холестерина - транспортная холестеринемия, сопровождающая транспортную гиперлипемию, г) изменение холестерино-протеинового комплекса в крови в результате нарушения белковых фракций, например при липоидном нефрозе, когда количество холестерина в крови может превышать 1%, д) нарушение окисления холестерина, наблюдаемое в связи со снижением функции щитовидной железы; введение же тироксина заметно уменьшает уровень холестерина в крови.
Вследствие нарушения холестеринового обмена и накопления холестерина в крови могут развиваться некоторые патологические процессы: отложение холестерина преимущественно в элементах ретикуло-эндотелия, так называемое анизотропное ожирение (С. С. Халатов). Возможно отложение холестерина в гистиоцитах кожи и сухожилий с реактивным разрастанием ткани (xanthomatosis). Отложение холестерина наблюдается при старческом помутнении роговицы (gerontoxon).
С нарушением холестеринового обмена связывают артерио- или атеросклероз. Под ними понимают утолщение внутреннего слоя сосудистой стенки, разрастание в нем соединительной ткани, развитие гиалиноза преимущественно в средних и мелких артериях, отложение липоидных веществ, особенно холестерина и его эстеров. Отложение холестерина наиболее выражено в стенках крупных сосудов.
Возникновение атеросклероза Н. Н. Аничков объясняет накоплением в крови вводимого с пищей холестерина и инфильтрацией им стенок сосудов. В его опытах кормление животных (кроликов) богатой холестерином пищей или холестерином, растворенным в масле, вызывало атеросклеротические изменения, сходные с атеросклерозом у человека. То же можно вызвать у собак с пониженной функцией щитовидной железы при кормлении их растворенным в масле холестерином. Стимуляция окислительных процессов тормозит развитие атеросклероза, например при длительном введении в организм витамина С или тиреоидина.
В настоящее время в патогенезе атеросклероза придается значение нарушению не столько экзогенного холестеринового обмена, сколько эндогенного: усилению синтеза холестерина или изменению коллоидного состояния его в плазме, т. е. нарушению липопротеиновых комплексов, что в свою очередь ставится в зависимость от изменений белковых фракций. Распад этих комплексов ведет к освобождению холестерина. Кроме того, в патогенезе атеросклероза большое значение имеет также изменение самой сосудистой стенки, развившееся вследствие интоксикации (при инфекционных воспалительных процессах или отравлении никотином), гемодинамических расстройств (при гипертонической болезни) или нарушения ее иннервации в связи с функциональным расстройством нервной деятельности. На развитие атеросклероза влияют также факторы психогенного характера.
С расстройством холестеринового обмена связано образование рад и арных холестериновых камней в желчном пузыре.
ПОИСК:
© ANFIZ.RU, 2011-2022
При использовании материалов сайта активная ссылка обязательна:
http://anfiz.ru/ 'Анатомия и физиология человека'
При использовании материалов сайта активная ссылка обязательна:
http://anfiz.ru/ 'Анатомия и физиология человека'